工業(yè)上用某礦渣(含有Cu2O��、Al2O3���、Fe2O3��、SiO2)提取銅的操作流程如圖:
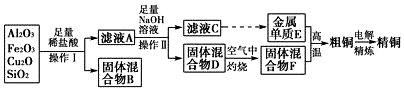
已知:Cu2O+2H+=Cu+Cu2++H2O.
(1)操作Ⅰ的名稱為
過(guò)濾
過(guò)濾
����;灼燒操作中常用的實(shí)驗(yàn)儀器有酒精燈、三腳架���,還有泥三角��、坩堝
泥三角��、坩堝
(夾持儀器不寫(xiě)).
(2)固體混合物B的主要成分為SiO2�����、Cu
SiO2�、Cu
(寫(xiě)化學(xué)式)����;濾液A中鐵元素的存在形式只能為 能為Fe2+,理由是Fe2O3與鹽酸反應(yīng)后生成的Fe3+與過(guò)量銅單質(zhì)反應(yīng)后��,全部轉(zhuǎn)化為Fe2+
Fe2O3與鹽酸反應(yīng)后生成的Fe3+與過(guò)量銅單質(zhì)反應(yīng)后,全部轉(zhuǎn)化為Fe2+
.檢驗(yàn)濾液A中Fe2+的試劑為硫氰化鉀溶液和新制氯水或鐵氰化鉀
硫氰化鉀溶液和新制氯水或鐵氰化鉀
(填試劑名稱).
(3)濾液中C鋁元素的主要存在形式為AlO2-
AlO2-
(填離子符號(hào))��,寫(xiě)出對(duì)應(yīng)的離子方程式Al3++4OH-=AlO2-+2H2O
Al3++4OH-=AlO2-+2H2O
.
(4)某同學(xué)認(rèn)為濾液NaAIO2的水解程度是微弱的����,AIO2-的水解不超過(guò)總量的10%,請(qǐng)?jiān)O(shè)計(jì)實(shí)驗(yàn)驗(yàn)證該同學(xué)的觀點(diǎn)是否正確用pH試紙測(cè)常溫下0.1mol?L-1NaAlO2溶液的pH����,若pH<12,則該同學(xué)的觀點(diǎn)正確����,若pH>12,則該同學(xué)的觀點(diǎn)錯(cuò)誤
用pH試紙測(cè)常溫下0.1mol?L-1NaAlO2溶液的pH����,若pH<12,則該同學(xué)的觀點(diǎn)正確��,若pH>12�,則該同學(xué)的觀點(diǎn)錯(cuò)誤
.
(5)從濃硫酸、濃硝酸����、蒸餾水中選用合適的試劑�,測(cè)定粗銅樣品中金屬銅的質(zhì)量分?jǐn)?shù)�,主要步驟:稱取一定質(zhì)量的樣品→將濃硫酸用蒸餾水稀釋,將樣品與足量稀硫酸充分反應(yīng)
將濃硫酸用蒸餾水稀釋����,將樣品與足量稀硫酸充分反應(yīng)
(填缺少的操作步驟���,不必描述操作過(guò)程的細(xì)節(jié))→過(guò)濾��、洗滌����、干燥→稱量剩余固體銅的質(zhì)量.


